Ottaa yhteyttä:Virhe Zhou (Herra.)
Puh: plus 86-551-65523315
Mobiili/WhatsApp: plus 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Sähköposti:sales@homesunshinepharma.com
Lisätä:1002, Huanmao Rakennus, Nro 105, Mengcheng Tie, Hefei Kaupunki, 230061, Kiina
Äskettäin julkaistussa kolmannen vuosineljänneksen taloudellisessa raportissaan Eli Lilly paljasti, että yritys on jättänyt uuden lääkehakemuksen (NDA) tirtsepatidille (LY3298176) Yhdysvaltain elintarvike- ja lääkeviranomaiselle (FDA), joka on kaksivaikutteinen lääke. GIP- ja GLP-1-reseptoriagonistit aikuisten tyypin 2 diabeteksen (T2D) hoitoon. Lisäksi yhtiö jätti myös tirtsepatidin myyntilupahakemuksen (MAA) Euroopan lääkevirastolle (EMA).
On erityisen syytä mainita, että samalla kun Eli Lilly toimitti NDA:n FDA:lle, hän lähetti myös Priority Review Voucherin (PRV) NDA-tarkistuksen nopeuttamiseksi. Nykyisen FDA:n prioriteettiarviointiaikataulun mukaan NDA:n tarkistusjakson odotetaan kestävän 8 kuukautta toimituspäivästä. Eli Lilly aikoo myös lähettää lisää listautumishakemuksia maailmanlaajuisesti vuoden 2021 loppuun mennessä.
Tirtsepatidi on Eli Lillyn kehittämä uudentyyppinen glukoosiriippuvainen insulinotrooppinen polypeptidi (GIP, joka tunnetaan myös nimellä mahalaukun estävä polypeptidi) ja glukagonin kaltainen peptidi-1 (GLP-1) -reseptori kaksoisaktivointi. Agentti. Sekä GIP että GLP-1 ovat suoliston erittämiä hormoneja, jotka voivat edistää insuliinin eritystä. Tirtsepatidi yhdistää kahden insuliinia edistävän vaikutuksen vaikutukset yhdeksi molekyyliksi ja edustaa uutta lääkeluokkaa tyypin 2 diabeteksen hoitoon.
Tirtsepatidi on tällä hetkellä vaiheen 3 kliinisen kehitysvaiheessa tyypin 2 diabeteksen hoitoon, painonhallintaan ja sydämen vajaatoiminnan hoitoon säilytetyllä ejektiofraktiolla (HFpEF). Lisäksi tirtsepatidia kehitetään myös mahdolliseksi lääkkeeksi alkoholittomaan steatohepatiittiin (NASH).
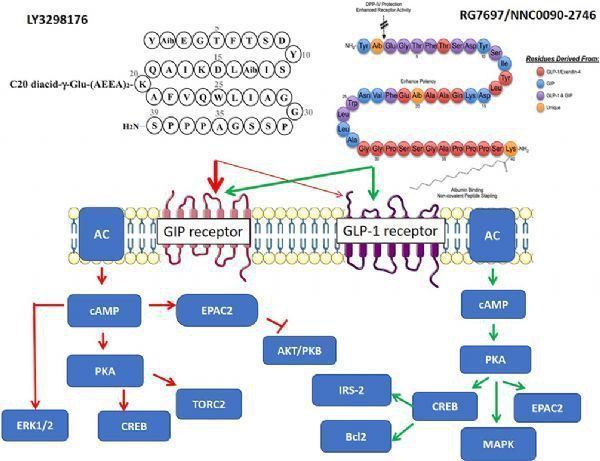
tirtsepatidi (LY3298176, kuva kirjallisuudesta: PMID-31686879)
Tirtsepatidin hakemusasiakirja tyypin 2 diabeteksen hoitoon perustuu maailmanlaajuisen kliinisen kehitysprojektin SURPASS Phase 3 -projektin tietoihin. Hankkeeseen on otettu yli 13 000 tyypin 2 diabetespotilasta 10 kliiniseen tutkimukseen, joista 5 on maailmanlaajuisesti rekisteröityjä tutkimuksia. Projekti käynnistettiin vuoden 2018 lopussa, ja kaikki viisi maailmanlaajuista rekisteröintikoetta on saatu päätökseen.
Juuri äskettäin tyypin 2 diabeteksen hoitoon tarkoitetun tirtsepatidin vaiheen 3 SURPASS-4 (NCT03730662) kliinisen tutkimuksen yksityiskohtaiset tulokset julkaistiin huippuluokan kansainvälisessä lääketieteellisessä lehdessä The Lancet. Katso tarkemmat tiedot: Tirtsepatidi vs. glargininsuliini tyypin 2 diabeteksessa ja kohonneessa kardiovaskulaarisessa riskissä (SURPASS-4): satunnaistettu, avoin, rinnakkaisryhmien monikeskustutkimus, vaiheen 3 tutkimus.
Tiedot osoittavat, että tyypin 2 diabetesta sairastavilla aikuispotilailla, joilla on suurentunut kardiovaskulaarinen (CV) riski verrattuna glargininsuliinititraukseen, kaikki kolme tirtsepatidin annosta osoittavat paremman verensokerin ja ruumiinpainon alentamisen: hoito 52 viikkoa, parantava vaikutus. Arvio (tehokkuus) estimand) tilastollinen analyysimenetelmä, suurin tirtsepatidin annos (15 mg, kerran viikossa) alentaa verensokeritasoa (A1C) lähtötasosta 2,58 % ja painoa 11,7 kg (25,8 naulaa, 13,0 %) lähtötasosta, ja titraa Insuliini glargiini alensi A1C-arvoa 1,44 % ja paino nousi 1,9 kg (4,2 lbs, 2,2 %) lähtötasosta.

SURPASS-4 tutkimusdata
SURPASS-4 on tähän mennessä suurin ja pisin tutkimus SURPASS-projektissa, ja se on myös viides ja viimeinen valmistunut maailmanlaajuinen rekisteröintitutkimus tirtsepatidista tyypin 2 diabeteksen hoitoon. Ensisijainen päätetapahtuma mitattiin 52 viikon kohdalla, ja potilaat jatkoivat hoitoa 104 viikon ajan tai kunnes tutkimus oli saatu päätökseen. Tutkimuksen loppuun saattamisen laukaisi merkittävien haitallisten kardiovaskulaaristen tapahtumien (MACE) kerääntyminen sydän- ja verisuonisairauksien riskin arvioimiseksi. Äskettäin julkaistuissa tiedoissa 52 viikon jälkeisestä hoitojaksosta tirtsepatidilla hoidetut potilaat säilyttivät A1C:n ja painonhallinnan jopa 2 vuoden ajan.
Tirtsepatidin kokonaisturvallisuus arvioitu koko tutkimusjakson aikana oli yhdenmukainen 52 viikon aikana mitattujen turvallisuustulosten kanssa, eikä uusia löydöksiä ollut 104 viikon aikana. Ruoansulatuskanavan sivuvaikutukset ovat yleisimmät haittatapahtumat, jotka yleensä ilmenevät annoksen nostamisen aikana ja sitten vähenevät ajan myötä.
Turvallisuusanalyysissä arvioitiin MACE-4 (sydän- ja verisuoniperäinen tai selittämätön kuolema, sydäninfarkti, aivohalvaus ja sairaalahoito epästabiilin angina pectoriksen vuoksi). SUPERSES-4-tutkimuksessa, jossa tirtsepatidia verrattiin glargininsuliiniin, tirtsepatidin ei havaittu lisääntyneen kardiovaskulaarisen riskin vuoksi; havaittu vaarasuhde (HR) oli 0,74 (95 % CI: 0,51-1,08), mikä on suotuisa tirtsepatidille.