Ottaa yhteyttä:Virhe Zhou (Herra.)
Puh: plus 86-551-65523315
Mobiili/WhatsApp: plus 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Sähköposti:sales@homesunshinepharma.com
Lisätä:1002, Huanmao Rakennus, Nro 105, Mengcheng Tie, Hefei Kaupunki, 230061, Kiina
Roche ilmoitti äskettäin, että Yhdysvaltain elintarvike- ja lääkevirasto (FDA) on hyväksynyt anti-PD-L1-hoidon Tecentriqin (atetsolitsumabi): vaiheen II-IIIA ei-pienisoluisen keuhkosyövän (NSCLC) hoitoon, jossa PD-L1 ≥ 1 % kasvaimen ilmentymistä aikuisille. potilaille adjuvanttihoitona leikkauksen ja platinapohjaisen kemoterapian jälkeen. Hyväksyntä perustuu Phase 3 IMpower010 -tutkimuksen tuloksiin. Tiedot osoittavat, että Tecentriq-adjuvanttihoito voi parantaa PD-L1-positiivisten vaiheen II-IIIA NSCLC-potilaiden sairaudesta vapaata eloonjäämisaikaa kolmella pisteellä verrattuna Best Supported Care (BSC) -hoitoon enemmän kuin yhdellä.
Adjuvanttihoidon tarkoituksena on vähentää uusiutumisen riskiä ja tarjota parhaat mahdollisuudet parantua. Siitä huolimatta noin puolet varhaisvaiheessa (vaihe I-II) tai paikallisesti edenneistä (vaihe III) NSCLC-potilaista uusiutuu lopulta saatuaan hoitoa parantavaa tarkoitusta varten. Adjuvanttiplatinapohjainen kemoterapia on tällä hetkellä tavallinen hoito-ohjelma potilaille, joilla on varhaisen vaiheen NSCLC (vaihe IB-IIIA), joilla on suuri riski taudin uusiutumisesta täydellisen resektion jälkeen. Verrattuna havaintoon, adjuvantti platinapohjainen kemoterapia voi lisätä 5 vuoden eloonjäämisprosenttia kohtalaisesti 4-5 %. Siksi tällä alalla on suuri tyydyttämätön lääketieteellinen kysyntä uusille adjuvanttihoidoille.
On syytä mainita, että Tecentriq on ensimmäinen ja ainoa syövän immunoterapia, joka on hyväksytty NSCLC:n adjuvanttihoitoon. Se aloittaa uuden aikakauden: varhaisen vaiheen keuhkosyöpään sairastuneilla potilailla on mahdollisuus saada syövän immunoterapiaa parantamaan paranemistaan. Mahdollisuus. Tämän päivän virstanpylväshyväksyntä tarjoaa lääkäreille ja potilaille uuden menetelmän varhaisen vaiheen keuhkosyövän hoitoon. Tällä uudella menetelmällä on potentiaalia vähentää merkittävästi syövän uusiutumisen riskiä. Yli kymmenen vuoden ajan alkuvaiheen keuhkosyövän hoidossa on edistytty vain vähän.
Tecentriq':n adjuvanttihoito PD-L1-positiiviseen varhaisen vaiheen NSCLC:hen on hyväksytty Yhdysvaltain FDA:n':n reaaliaikaisen onkologian katsauksen (RTOR) pilottiprojektissa ja Orbis-projektissa. RTOR-projektin tavoitteena on tutkia tehokkaampaa arviointiprosessia varmistaakseen, että potilaat saavat turvallisen ja tehokkaan hoidon mahdollisimman pian. Orbis-hankkeen tavoitteena on tarjota puitteet onkologisten tuotteiden yhteiselle toimitukselle ja hyväksymiselle Yhdysvaltain FDA:lle ja sen kansainvälisen yhteistyön sääntelyvirastoille, nopeuttaa tarkistusprosessia ja saavuttaa syöpälääkehakemusten samanaikainen hyväksyntä eri maissa.
Bonnie Addario, GO2-säätiön perustaja ja puheenjohtaja, sanoi: "Liian monilla varhaisvaiheen keuhkosyöpää sairastavilla potilailla sairaus uusiutuu leikkauksen jälkeen. Nyt immunoterapia leikkauksen ja kemoterapian jälkeen antaa monille potilaille uutta toivoa ja vahvan uuden näkemyksen. Työkaluja syövän uusiutumisen riskin vähentämiseen. Tämän hyväksynnän ansiosta on tärkeämpää kuin koskaan seuloa keuhkosyöpä varhaisessa vaiheessa ja havaita PD-L1 diagnoosin yhteydessä, jotta tämä edistys saataisiin hyödyksi."
IMpower010 kliiniset tiedot
IMpower010 on maailmanlaajuinen, monikeskus, avoin, satunnaistettu vaiheen 3 tutkimus, jossa arvioidaan potilaita, joilla on vaiheen IB-IIIA NSCLC (UICC-versio 7) kirurgisen resektion ja jopa 4 sisplatiinipohjaisen adjuvanttikemoterapian jälkeen. Teho ja turvallisuus. Tecentriqin ja BSC:n käytöstä adjuvanttihoidossa. Tässä tutkimuksessa 1 005 potilasta jaettiin satunnaisesti suhteessa 1:1, ja heille annettiin jopa 16 Tecentriq- tai BSC-kurssia. Ensisijainen päätetapahtuma: PD-L1-positiivinen vaiheen II-IIIA potilaspopulaatio, kaikki satunnaistettu vaiheen II-IIIA potilaspopulaatio, IB-IIIA-potilaspopulaatio (ITT) ja sairaudesta vapaa eloonjääminen (ivDFS), jonka tutkija on määrittänyt ) . Keskeisiä toissijaisia päätepisteitä ovat: kokonaiseloonjääminen (OS) koko tutkimuspopulaatiossa, ITT IB-IIIA NSCLC -potilaspopulaatio. Tulokset osoittavat, että:
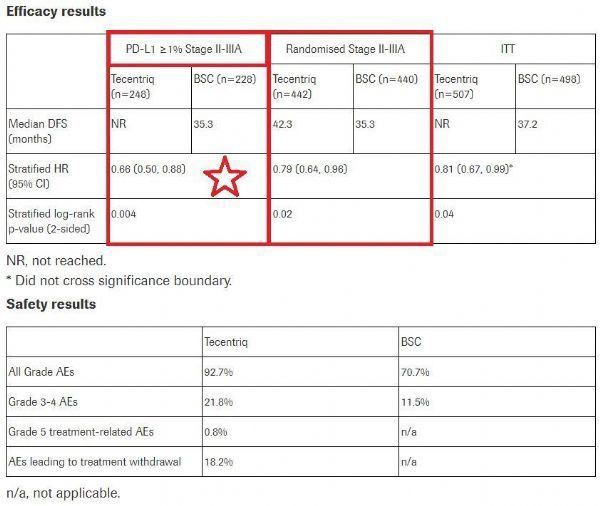
——Potilailla, joilla on vaiheen II-IIIA NSCLC, joiden kasvaimet ilmentävät PD-L1≥1 %: Leikkauksen ja kemoterapian jälkeen, kun Tecentriqia käytetään adjuvanttihoidossa BSC:hen verrattuna, taudin uusiutumisen tai kuoleman riski pienenee merkittävästi 34 %. (HR=0,66; 95 % CI: 0,50 - 0,88; p=0,004). Tässä potilaspopulaatiossa DFS:n mediaani Tecentriq-hoitoryhmässä ei ole saavutettu, ja DFS:n mediaani BSC-ryhmässä on 35,3 kuukautta.
——Kaikilla satunnaistetuilla vaiheen II-IIIA NSCLC-potilailla: Keskimääräisen 32,2 kuukauden seurannan jälkeen Tecentriq vähensi taudin uusiutumisen tai kuoleman riskiä 21 % verrattuna BSC:hen (HR=0,79; 95 %:n luottamusväli: 0,64–0,96); P=0,02). Tässä potilaspopulaatiossa DFS:n mediaani pidentyi Tecentriq-ryhmässä 7 kuukaudella BSC-ryhmään verrattuna (42,3 kuukautta vs. 35,3 kuukautta).